
金屬鋰作為鋰二次電池負極,兼具超高比容量和非常低的電化學電位的優點。然而,鋰枝晶生長帶來的安全性問題以及副反應等,很大程度上限制了鋰金屬負極的應用。研究表明,通過以下幾種方法可以在一定程度上緩解枝晶生長等相關問題:
(1) 具有較低Cs+濃度的電解質可以消耗低電流下生長的枝晶。
(2)電解質添加劑、高的鋰鹽濃度、 預處理、人工非原位修飾等。但是,大多數在鋰表面形成保護層的手段,都會造成電子/離子電導率和機械穩定性降低,而且僅在數百次的低電流循環下才有效。
在這里,加拿大滑鐵盧大學Linda F. Nazar 教授課題組報道了一種非常高效的方法抑制鋰枝晶——在金屬Li表面通過原位形成由鋰基合金(Li13In3, LiZn, Li3Bi或者Li3As)組成的表面膜,表現出較快的離子遷移速率。
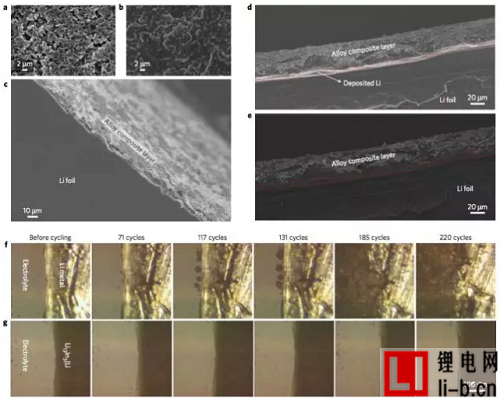
圖1. 合金保護鋰金屬的掃描電子顯微鏡和光學顯微鏡圖像研究。
a和b分別是新鮮鋰金屬(a)和Li13In3|Li復合負極(b)在2mAh/cm^2下的圖像; Li13In3|Li復合負極在未電鍍前的截面圖像(c),Li13In3|Lii復合負極在2mAh/cm^2下的橫截面圖(d)以及相應的背散射電子模式圖像(e), d和e中的紅色虛線勾勒出電沉積的Li;新鮮的鋰(f)和復合Li13In3|Li電極(g)在對稱透明電池光學顯微圖像。
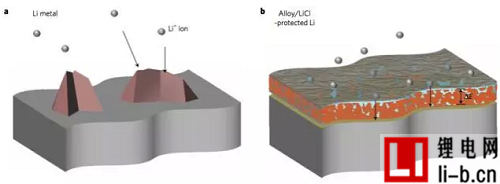
圖2. 示意圖描述了合金保護的鋰箔的功能。
a, 無保護的鋰箔經受枝晶生長;b,合金/LiCl保護的Li箔s上形成電位梯度的保護層(E),并且通過~10μm膜具有良好的界面增強Li+電荷轉移能力,這兩個因素都抑制枝晶生長;(b)中的陰影橄欖區是界面,合金相和非晶/納米晶體LiCl相分別以橙色和淺藍色表示.
得益于高導電性的富鋰合金膜和電子絕緣的副產物LiCl二者的協同作用,該鋰金屬電極表現出優異的電化學性能。在2mA/cm^2下可穩定循環達700次(1400小時),并且在與Li4Ti5O12(LTO)電極配對時,以5C倍率(1C=1Li/h)可穩定循環1500次。對循環后的材料進行非原位SEM測試,發現在合金層下發生了Li沉積現象,由此表明該方法得到的富鋰合金可以有效改善鋰枝晶的生成問題。
合成步驟:
鋰保護電極制備:在小于1ppm氧氣和濕氣的氬填充手套箱中,將鋰金屬箔(99.9%,Aldrich)拋光至表面發光。拋光后,將鋰箔浸入在含有0.167M MClx的四氫呋喃(THF)溶液中20秒(M = As,In,Zn或Bi)。從THF溶液中取出后,小心地除去鋰箔上過量液體。然后將箔用THF漂洗,在室溫下真空干燥兩天,并切成11mm圓形,用于電化學電池中的研究。
Li13In3體相制備:銦箔和鋰箔在使用前進行拋光。測量所需量的箔堆疊在一起。在12mm直徑的模具中,用4噸壓力壓制疊層箔30分鐘。所有步驟都在Ar填充的手套箱中進行。
來源:能源學人,標題有更改





